Загадковий бензол
У великому світі органічної хімії лише деякі сполуки мають настільки бурхливу «біографію», як бензол. Протягом багатьох десятиліть ця речовина була предметом нескінченних суперечок хіміків-теоретиків, об’єктом пильної уваги і свого роду каменем спотикання класичної хімії. І навіть сьогодні, в століття небувалого проникнення науки в таємниці будови матерії, бензол та його похідні продовжують підносити дослідникам сюрпризи.
Історія відкриття бензолу
Бензол був відкритий Майклом Фарадеєм. В 1823 році, будучи ще скромним лаборантом Королівського інституту в Лондоні, він поставив серію дослідів по зрідження газів і першим довів, що під впливом тиску і низьких температур вони здатні перетворюватися в рідині. Пізніше, в 1825 році, сжижаючи світильний газ, Фарадей виділив безбарвну маслянисту рідину з характерним запахом, киплячу під нормальним тиском при температурі +80 градусів. Аналіз хімічного складу показав, що молекули нової речовини складаються з шести атомів вуглецю і такого ж числа атомів водню, що дає хімічну формулу С6Н6. Це був бензол, який став родоначальником цілого класу органічних сполук, відомих під назвою ароматичних.
Вже незабаром після відкриття бензол перестає бути тільки лабораторною речовиною (як саме отримання бензолу перестає бути проблемою) — його навчилися одержувати в досить великих кількостях з продуктів сухої перегонки кам’яного вугілля,— і хіміки приступають до ретельного вивчення властивостей нового з’єднання, що опинилося вельми реакційно здатним. Так, наприклад, бензол активно вступав в реакцію з багатьма кислотами, взаємодіючи з однією з яких, азотною, утворював нітробензол C6H5N02. У 1842 році професор Казанського університету Микола Миколайович Зінін отримав з нітробензолу анілін (C6HSNH9), і це відкриття стало «відправним пунктом» історії незабаром бурхливо розвиненої анілофарбної промисловості.
Освоєння синтезу анілінових барвників було одним із заключних «акордів» хаотичного розвитку хімії першої половини позаминулого століття. До цього часу стало остаточно ясно, що для подальшого руху вперед необхідна загальна хімічна теорія, здатна з єдиних позицій розглянути розрізнені факти, накопичені дослідниками. У створенні такої теорії вирішальна роль належить видатному хіміку Олександру Михайловичу Бутлерову. У 1861 році на з’їзді природознавців і лікарів в Шпейере (Німеччина) Бутлеров доповів основи своєї теорії будови, яка встановлює взаємозв’язок між властивостями речовин і структурою їх молекул. Формулюючи цю теорію, вчений виходить з уявлень про чотирьохвалентність атомів вуглецю і їх здатності з’єднуватися один з одним, утворюючи прямі і розгалужені ланцюги.
Теорія Бутлерова пояснювала явище ізомерії, що складається у відмінності властивостей сполук з однаковим хімічним складом, але різною будовою молекул, розкривала механізм підвищеної активності неграничних вуглеводнів, молекули яких містили подвійні і потрійні зв’язки. Більше того, виходячи з цієї теорії, можна було передбачити властивості сполук, які до цього часу ще не були відкриті.
Справедливість теорії будови підтверджувалася численними експериментальними даними. А між тим бензол і його похідні вперто не вкладалися в її логічні рамки. Власне, збудувати шість атомів вуглецю в прямий ланцюг і наситити вільні валентності шістьма атомами водню не представляло особливих труднощів. Але тоді виявлялося, що реальні хімічні властивості бензолу і ті властивості, які, згідно з теорією будови, повинні були б мати з’єднання з подібною структурою молекул, різко відрізняються один від одного.
Наприклад, згідно з теорією будови, сполуки, в молекулах яких містяться потрійні зв’язки, повинні активно приєднувати галогени — хлор, бром, йод. Бензол взаємодіяв з галогенами, але при цьому йшла реакція заміщення атомів водню атомами галогенів, а не реакція приєднання. Крім того, в приведеній в якості прикладу лінійній формулі властивості крайніх атомів вуглецю повинні бути іншими, ніж у середніх. А накопичені хіміками факти говорили про те, що в молекулі бензолу всі атоми вуглецю рівноцінні. Почалися пошуки будови молекул бензолу, що відповідає його властивостям. Цю задачу вдалося вирішити німецькому хіміку Августу Фрідріху Кекуле.
Важко сказати, що послужило поштовхом, який призвів Кекуле до його відкриття, — біографи і сучасники сходяться на тому, що думка про циклічну будову молекул бензолу прийшла до вченого під час його перебування в Англії в кінці 1864 року. Одностайно вказується і місце зародження ідеї — вагон омнібуса, в якому Кекуле перетинав Лондон, повертаючись з бібліотеки. Але далі думки розходяться: одні стверджують, що з вікна вагона вчений побачив клітку з мавпами, що схопилися лапами одна за одну і утворили замкнуте кільце, інші,— що він задрімав в омнібусі, і йому наснилися вуглецеві ланцюги у вигляді химерних змій, одна з яких раптом закусила свій хвіст. Чи так було насправді чи інакше, але на початку 1865 року вийшла в світ робота Кекуле, в якій він на підставі теоретичних і експериментальних даних робив висновок про циклічну будову молекули бензолу і пропонував її структурну формулу у вигляді шестикутника.
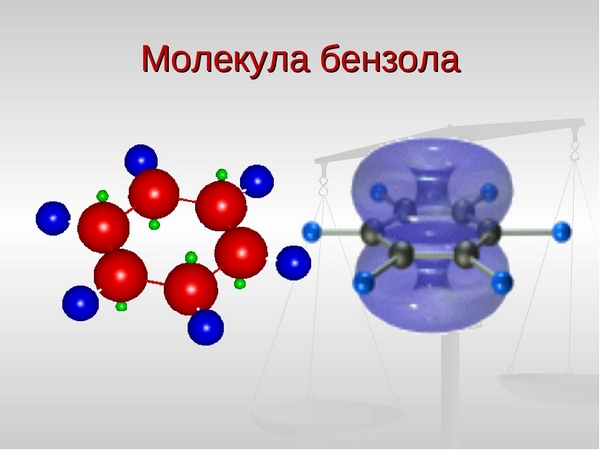
Приблизно так виглядає молекула бензолу.
Відкриття Кекуле, безперечно, було одним з найбільш видатних досягнень хімії XIX століття, воно стало першим кроком до визнання можливості існування циклічних структур органічних сполук не тільки шестикутної, але й іншої геометричної конфігурації. Формула Кекуле пояснювала багато чого з того, що було загадковим у поведінці бензолу і його похідних. І, тим не менш, хіміків вже тоді бентежили її недоліки, основною причиною яких були подвійні зв’язки, що входять у формулу.
Один з недоліків формули Кекуле проявлявся при розгляді так званих дизаместителів бензолу — його похідні, в молекулах яких два атоми водню були замінені атомами інших елементів або групами атомів. Прикладом такого дизаместителя може служити ортодихлорбензол — похідний бензолу, у молекулі якого два сусідні атоми водню заміщені атомами хлору. Якщо допустити, що формула Кекуле вірна, то це означає, що повинні існувати два види ортодихлорбензола з різними хімічними властивостями: один — з атомами хлору, розташованими по кінцях одинарного зв’язку, й інший — з атомами хлору на кінцях подвійного зв’язку. Тоді в сумі з двома іншими похідними бензолу — парадихлорбензолом і метадихлорбензолом — загальне число можливих дизаместителів повинне дорівнювати чотирьом. А між тим самі строгі методи аналізу дозволяли встановити наявність лише трьох дизаместителів і наполегливо відмовляли у «праві громадянства» четвертому.
Природно, недоліки формули Кекуле (а вони не обмежувалися наведеним прикладом) не могли не викликати пошуків більш досконалих структур молекули бензолу. Одну з перших таких спробу зробив англійський хіміко-фізик Джеймс Дьюар, який запропонував у 1867 році свою формулу у вигляді шестикутника, але вже тільки з двома подвійними зв’язками. Залишений вільним одинарний зв’язок поєднував в цій формулі протилежні вершини фігури. Але, будучи оригінальним рішенням, формула Дьюара грішила ще більш серйозними недоліками: вона дозволяла представити вже шість різних дизаместителів бензолу і плюс до них два монозаместителя (приставка «моно» означає «один»). Насправді ж бензол давав лише одне з’єднання з заміщених, наприклад, тим же хлором одним з атомів водню, і цю властивість відображала формула Кекуле, в якій всі вершини шестикутника були рівноцінними. Не дивно тому, що формула Дьюара не отримала визнання і незабаром була віддана забуттю.
Як формула Кекуле, так і формула Дьюара мали загальний недолік — «мертві» подвійні зв’язки. Вище вже говорилося, що, згідно з теорією будови, наявність в молекулі органічної сполуки непредільності (подвійних або потрійних зв’язків) має виявлятися в приєднанні атомів галогенів, що не було властиво бензолу і його похідним. Таким чином, сам факт існування подвійних зв’язків в молекулі бензолу ставився під сумнів, плодом якого була поява в 1869 році формули Ладенбурга.
Відмовившись від уявлення про молекулу бензолу як про плоске тіло, німецький хімік, професор Гейдельберзького університету Альберт Ладенбург запропонував характеризувати її будову з допомогою тригранної призми, у вершинах якої розташовувалися сполучені одинарними зв’язками атоми вуглецю. Без подвійних зв’язків формула Ладенбурга, подібно формулі Кекуле, дозволяла представити лише один варіант монозаместителя і, на жаль, чотири різних дизаместителя. Але разом з тим їй був притаманний і «фатальний недолік». Відомо, що молекула сполуки, званої нафталіном, складається з двох зрощених кілець бензолу. Коли ж у молекулі нафталіну хіміки намагалися «зростити» дві призми Ладенбурга, то виходила неймовірна річ: загальні для зрощених молекул атоми вуглецю виявлялися… п’ятивалентними. Зрозуміло, що змусити хіміків примиритися з таким «нововведенням» було досить важко.
Формула Ладенбурга була далеко не останнім із запропонованих різними дослідниками варіантів будови молекули бензолу. Протягом наступних років одна за одною виникали формули, що перетинають шестикутник зв’язками, прикладом яких може служити формула німецького хіміка Клауса і навіть формула зі зв’язками, кінці яких повисали в просторі — хіміки йшли навіть на такі хитрощі, щоб позбавитися від злощасних подвійних зв’язків. Але всі ці структури спіткала та ж доля — вони не отримали визнання, залишивши поле битви за піонером — формулою Кекуле.
Втім, остання теж не залишилася незмінною: бачачи недосконалість свого дітища, Кекуле висунув на початку 90-х років позаминулого століття так звану гіпотезу осциляції, згідно з якою інертність подвійних зв’язків в молекулі бензолу пояснювалася тим, що вони безперервно змінюються місцями з одинарними. Але, виключивши одне протиріччя, ця гіпотеза призводила до іншого: виходило, що в одного і того ж з’єднання можуть бути дві різні структури…
Це був один з найбільш яскравих симптомів — класична хімія XIX століття опинилася перед обличчям кризи. А звідси не забарилася послідувати і відмова від звичних уявлень, результатом якого була поява формули Тіле, співвітчизника Кекуле. Відмовившись від пануючої тоді думки про те, що хімічні зв’язки можуть характеризуватися лише цілими числами, Тіле поєднав вуглецеві атоми молекули бензолу полуторними зв’язками, позначивши додаткові половинчасті зв’язку між атомами замкнутою пунктирною лінією всередині шестикутника. Як з’ясувалося пізніше, структура німецького вченого разюче схожа на реальну, але її поява у великій мірі була лише плодом інтуїції, підкріпити яку жодними фактами Тіле в той час не міг. І тільки в 20-х роках минулого століття з розвитком нової галузі науки — квантової хімії, будова молекули бензолу перестала бути загадкою.
Властивості бензолу: фізичні і хімічні
Союз з фізикою виявився дуже плідним для хімії бензолу: використовуючи фізичні методи дослідження, хімікам вдалося проникнути в глибини будови цього вуглеводню. Так, наприклад, рентгеноструктурний аналіз показав, що молекула бензолу являє собою плоский шестикутник і, отже, просторова формула Ладенбурга неспроможна.
Спектральний аналіз дозволив з’ясувати, що молекула бензолу має вісь симетрії шостого порядку (або, іншими словами, що її властивості в напрямку всіх шести атомів однакові), виключивши тим самим формулу Дьюара. А використовуючи фізичні методи розрахунку, хіміки встановили, що в молекулі бензолу атоми вуглецю відстоять один від одного на відстані 1,4 ангстрема, в той час як одинарним зв’язкам відповідає відстань в 1,54 ангстрема, а подвійним — в 1,34 ангстрема. Виходило, що зв’язки між бензольними атомами вуглецю представляють собою щось середнє між подвійними та одинарними. Залишалося з’ясувати природу цих зв’язків, суть якої полягає в наступному.
З точки зору сучасних уявлень хімічний зв’язок між двома атомами обумовлений взаємодією електричних і магнітних полів електронів, що належать їм . При цьому для утворення кожного одинарного зв’язку необхідно два електрона — по одному від кожного атома. Оскільки електрони перебувають у безперервному русі, їх положення в просторі прийнято характеризувати за допомогою так званих «хмар ймовірності», або «електронних хмар». У міру віддалення від ядра атома ймовірність знаходження електрона в даній точці простору зменшується, і цю обставину зазвичай відображають на схемах з допомогою більш рідкісного штрихування.
Простий одинарний хімічний зв’язок (наприклад, між атомами в молекулі водню) називається сигма-зв’язком (о-зв’язок) і утворюється в результаті взаємодії так званих s-електронів. Хмари цих електронів мають форму кульок з нескінченно великим радіусом, центри яких збігаються з ядрами атомів. Для утворення сигма-зв’язку необхідно, щоб хмари s-електронів частково перекривали один одного.
Факт перекриття електронних хмар є обов’язковою, але в той же час ще недостатньою умовою виникнення зв’язку. Крім того, що кожен електрон рухається навколо ядра атома, він ще обертається навколо власної осі і, як прийнято говорити у фізиці, характеризується власним моментом обертання, або спіном («спін» в перекладі з англійської означає «веретено»). При цьому, згідно з законами квантової механіки, зв’язок між атомами виникає лише в тому випадку, коли спіни їх електронів направлені в протилежні сторони, що на схемах зображують антипараллельними стрілками.
Якщо ж два атоми з’єднані між собою двома зв’язками (наприклад, атоми вуглецю в молекулі етилену), то тільки один з них є сигма-зв’язком. Другий ж зв’язок утворюється парою так званих р-електронів з антипараллельними спінами, електронні хмари яких вже мають іншу форму — вони нагадують посудину пісочного годинника або дві складених вістря до вістря краплі, що в перерізі дають плоску вісімку. Хімічний зв’язок, що виникає при перекритті цих хмар дещо слабше сигма-зв’язку і носить назву пі-зв’язку (л-зв’язок).
В ще більш складній «конструкції», наприклад, у молекулі ацетилену, де атоми вуглецю з’єднані трьома зв’язками, один з них є сигма-зв’язком, а два інших — пі-зв’язками. При цьому осі симетрії хмар р-електронів лежать у площині, перпендикулярній сигма-зв’язку, і одночасно перпендикулярні один одному. На структурних схемах хмари р-електронів зазвичай зображуються стрілками, спрямованими вздовж осі симетрії відповідної хмари, в ту ж сторону, що і стрілки, що характеризують спіни електронів.
У порівнянні з останньою «конструкцією» структура молекули бензолу зовні виглядає простіше — її атоми вуглецю з’єднані між собою лише одним сигма – і одним пі-зв’язком. При цьому осі хмар я-електронів розташовані перпендикулярно до площини шестикутника, утвореного атомами вуглецю. Але ця простота позірна: подвійні зв’язки в молекулі бензолу та, наприклад, в молекулі етилену — це далеко не одне і те ж. Справа в тому, що р-електрони володіють високою рухливістю, яка в тісних рамках молекули етилену не може проявитися.
Інше — молекула бензолу. В ній накладання хмари р-електронів утворюють замкнутий «тунель», за яким електрони можуть переміщатися від одного атома до іншого. В результаті всі шість р-електронів перестають належати своїм атомам, або, як прийнято говорити, делокализуються і починають рухатися по всьому кільцю молекули. Цим «гуртуванням» р-електронів і пояснюється той факт, що зв’язки між атомами в молекулі бензолу займають проміжне положення між подвійними та одинарними. Дещо інакше утворюються в молекулі бензолу і сигма-зв’язки. Електронні хмари, при перекритті яких вони виникають, тут мають вже іншу форму, а центри кругових проекцій цих хмар на площину молекули зрушені по відношенню до атомів вуглецю.
Після затвердження в хімії квантовомеханічних уявлень про будову бензолу і характер зв’язків між його атомами, здавалося, що з цим питанням покінчено назавжди. Але ось у 1962 році американські хіміки Е. Тамелен, Б. Паппа та П. Паппа при опроміненні ультрафіолетовими променями одного з похідних бензолу — так званого тритретбутилбензола — отримали речовину з відмінними від вихідного продукту властивостями. Вивчення нового з’єднання показало, що воно є похідним ізомеру бензолу, що має… структуру Дьюара.
А через два роки з’єднання з аналогічною будовою кільця отримали німецькі хіміки Р. Кріге та Ф. Цанкер. Правда, отримана бензольна «конструкція» не зовсім відповідала формулі Дьюара — вона являла собою вже не шестикутник, а просторову фігуру, подібну відкритій книзі. Але зате в ній в повній відповідності з формулою Дьюара були два подвійні і один діагональний одинарний зв’язок.
Ще більш несподіваним виявився результат, отриманий бельгійськими вченими X. Віхе, Р. Жилеттом, В. Отом і Р. Мерені. Досліджуючи перетворення складного органічного з’єднання, відомого під назвою третичнобутилфторацетилена, вони зуміли виділити відразу три нових ізомери бензолу. Один з цих ізомерів представляв собою кристалічне з’єднання, що плавилось при температурі 187 градусів. Вивчення його будови показало, що цей ізомер має… призматичну структуру Ладенбурга, в силу чого і отримав назву призмана.
Другий виділений ізомер бензолу виявився рідиною, киплячою під тиском в 11 міліметрів ртутного стовпа при температурі 140 градусів. Будова молекул цього ізомеру не була схожа ні на одну з раніше пропонованих структур, і з-за відсутності аналогів це з’єднання отримало назву бензвалена. В процесі нагрівання, при температурі 220 градусів, цей ізомер перетворювався на з’єднання, що має структуру Кекуле. Нарешті, третій з отриманих вченими ізомерів мав будову, що відповідає формулі Дьюара. Правда, цей ізомер бензолу був малостійким і швидко перетворювався в структуру, що відповідає формулі Кекуле. Але факт залишається фактом — всі три «конкуруючі» структури, дві з яких, здавалося, назавжди віддані забуттю, а третя збереглась лише в силу традиції, раптом знайшли реальний сенс через майже сто років після того, як були запропоновані.
Важко сьогодні прогнозувати, що дасть хімії відкриття нових ізомерів — вивчення їх властивостей практично тільки починається. Але те, що з їх появою в «біографії» бензолу відкрилася нова сторінка,— це безперечно.
Автор: М. Нейман.

