Хімічна стійкість речовини

Коли наука була молода, вона забороняла своїм лицарям лише одне — задавати питання «навіщо мені це знати?». І не задавали — розуміли: це ганебно, це табу. Але ось наука чогось досягла, обзавелася теорією, дозріла, і табу розмножилися. Адже кожне велике досягнення теорії вводить у науку свої заборони. Відкрили закон збереження енергії, він же перший початок термодинаміки, — закрили «тематику» тих, хто винаходив перпетуум мобіле, вічні двигуни; пояснили суть Періодичного закону — підрізали крила всім, хто мріяв відкрити елементи легше гелію, але важче водню; додумалися до хвильової природи елементарних частинок — розбили надії тих, хто намагався виміряти точну швидкість електрона.
Знання напам’ять всіх табу — це, мабуть, і є та ознака, за якою відрізняють вченого-професіонала від дилетанта: той, для кого фізика — професія, з вічним двигуном не возиться. Але скільки ж дилетантизму породжує на світ та обставина, що в міру дозрівання науки все менш обов’язковим для вченого стає табу номер один — «навіщо мені це знати?»! Занадто багато обзаводяться лише власними вузькими смужками на неосяжному полі знання — і тільки на ній кожен оре, сіє, збирає врожай. А що там на сусідніх ділянках — не його справа. Зіткнувшись ж з проблемою, яка не вписується в одну ділянку, вузький спеціаліст мимоволі потрапляє в положення дилетанта. Крім того, при цьому виникають свої, місцеві табу. Іноді абсолютно необґрунтовані, але вони лежать на шляху науки, поки не з’явиться рішуча людина, здатна орати широко або навіть орати поперек.
Є цікава книга — «Вічний рух», повчальна історія божевільної ідеї перпетуум мобіле, що століттями збирала під свої знамена цілі легіони майстерних винахідників, маніяків і шарлатанів. І ясно випливає з цієї історії, що не одну тільки шкоду принесли науці незліченні варіанти нав’язливої ідеї. Ламаючи над нею голови, ентузіасти по ходу справи винайшли чимало справді корисних речей. В моїй науці, хімії, теж є свої завдання, які зажили слави нерозв’язних, але тим і приваблюють горді розуми, свої «вічні двигуни», іноді нездійсненні, іноді реалізовані, але на перевірку зовсім не вічні, — так само як годинник, що ніколи не зупинявся одного хитромудрого англійця, він заводився рухом ртутного стовпа в барометрі. Ось про цю боротьбу за неможливе, мабуть, неминучу в будь-якій області знання, я і розповім.
Речовина, якої бути не повинно
Можлива молекула, в якій атоми вуглецю розташовані ось так:
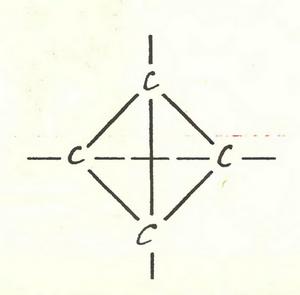
По-перше, кути між зв’язками тут занадто малі — велика напруга зв’язків, молекула її не витримає. По-друге, ті ж атоми можна розташувати іншим, більш стійким чином. Ось вони і розташуються, вас не запитають. Ну а третє, найголовніше,— до сих пір таких молекул не міг отримати ніхто, хоча за справу бралися не дурні. Виходить, їх бути не повинно.
Заперечення такого роду довго доводилося вислуховувати ентузіастам, які намагалися синтезувати тетраэдран — речовину, в молекулі якої чотири атоми вуглецю утворюють правильну піраміду.
В точності ті ж резони обрушувалися на мрійників, які мріяли про циклобутадієн — речовину, молекула якої має ось такий каркас:
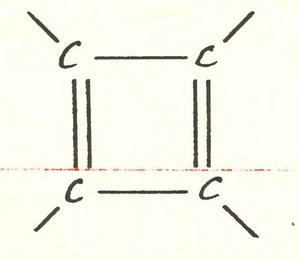
До того ж пригнічували цих мрійників ще одним, справді серйозним аргументом. Теорія забороняє таку комбінацію з подвійних і ординарних зв’язків. Один з подвійних обов’язково буде розірваний, і молекула набуде властивості вільного радикала. А більшість радикалів існує лише незначні частки секунди. Значить, і циклобутадієна бути не повинно.
Тим не менш і тетраэдран, і циклобутадієн після багаторічних мук і суперечок все ж були синтезовані. Вдалося підібрати такі групи атомів, з яким атоми вуглецю зв’язані своїми четвертими валентностями (на схемах ці групи не показані), так що речовини вийшли порівняно стійкими. Неможливе стало можливим — такий собі невеликий «вічний двигун».
Так, може, і табу, що відноситься до перпетуум мобіле, теж вдасться об’їхати? Е, ні, закони термодинаміки, що забороняють перпетуум мобіле, мають незаперечну силу, а тут були табу місцеві, якщо хочете, відомчі. Та й обійшли їх, чесно кажучи, лише умовно: ці героїчним чином отримані сполуки можна вважати стійкими в тій же мірі, в якій вважати вічним двигуном гіроскоп, який буде обертатися тиждень або навіть місяць, але, врешті, решт, все одно зупиниться.
Коли хіміки кажуть: речовина стійка, це зовсім не означає, що з нею нічого не зробиться при п’яти тисячах градусів або з тиском мільйон атмосфер. Мало того, це не значить, що речовина буде існувати вічно при кімнатній температурі. В лабораторному побуті прийняті мірки прості, життєві. Якщо речовина вважається стійкою, це просто означає, що вона може прожити при кімнатній температурі, хоча б кілька днів. Тому що не можна плутати між собою два зовсім різних поняття: стійкість і здатність до існування. Якщо розібратися, так само, як не можна прийняти за вічний двигун будь-яке обертове колесо.
Навіть якщо хімік педантично уточнює: дане з’єднання, мовляв, стійке при таких-то умовах, цього ще недостатньо. По-справжньому стійким можна вважати те угруповання атомів, при побудові якого енергія виділяється; і друга умова — ці атоми не можна зібрати в інше угруповання, при побудові якого енергії виділиться ще більше, по суті, це той самий перший початок термодинаміки, тільки прикладений до молекул.
— Ось вам і ознака! — вигукне квапливий любитель заборон. Ті речовини, молекули яких енергетично вигідні, синтезувати можна. А решта — табу! Теорія не велить.
Яким нудним було б ремесло хіміка, якби справа йшла так! Звичайно, закони термодинаміки непорушні, але є у неї властивість, що життя хіміків сильно прикрашає. Термодинаміка абсолютно байдужа до термінів виконання своїх розпоряджень. Рухоме колесо, що не отримує енергії ззовні, неминуче зупиниться. Може, через секунду, може, через рік, але зупиниться. Енергетично невигідна молекула теж неминуче розпадеться з виділенням «зайвої» у порівнянні з більш вигідними станом енергії. Розпадеться. Але коли?
Такі загальновідомі з’єднання, як ацетилен або оксид азоту (NO), термодинамічно нестійкі: енергія виділяється не при утворенні їх, а, навпаки, при розпаді на елементи. Тому якщо просто почекати досить довго біля балону з ацетиленом, то ніякого ацетилену в ньому, зрештою, не виявиться, а тільки вуглець і водень. Чому ж ацетилен існує? Та тому, що на таке «очікування у балона» не вистачить людського життя: розпад ацетилену йде надзвичайно повільно. Речовини, що в життєвому сенсі стійкі, а в термодинамічному — ні, досить поширені. Їх називають метаетабільними, або кінетично стійкими (від імені кінетики — науки про швидкості реакцій).
До числа таких «житейськи стійких» належать і тетраэдран з циклобутадієном, про яких йшла мова. Хіміки зуміли сильно уповільнити їх перехід в інші, енергетично вигідні системи. Ось і весь секрет.
Нерідко говорять, що синтез — не стільки наука, скільки мистецтво. Так не в тому чи це мистецтво полягає, щоб балансувати між термодинамікою і кінетикою? Мабуть, так. Що може завадити хіміку, здатному підібрати відповідні умови синтезу і подальшого зберігання речовини, виготовити майже будь-яку молекулу, зображення якої намалює його фантазія? При майстерно підібраних умовах речовина виявиться відчутною, існуючою, нестійка виявиться (умовно) стійкою, і в життєвому сенсі слова виявиться реалізованим майже будь-який хімічний «перпетуум мобіле». І саме в цьому криється серйозна небезпека.
«Навіщо мені ця теорія!»
Структурну формулу добре відомого вуглеводню бензолу можна зобразити так:
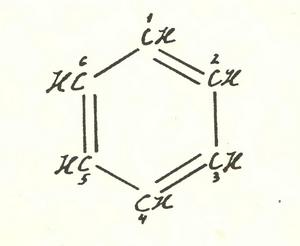
Або так.
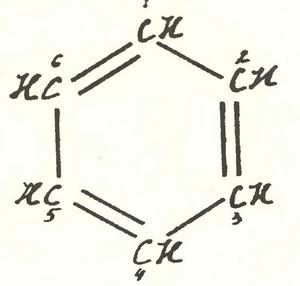
У першому варіанті подвійні зв’язки з’єднують атоми вуглецю, позначені номерами 1 і 2, 3 і 4, 5 і 6. У другому — 2 і 3, 4 і 5, 6 і 1. Різні формули? Різні. Значить, їм повинні відповідати різні речовини. До цього додумалися ще в позаминулому столітті, і на поділ «ізомерів» якщо не самого бензолу, то його родичів — ізомерів, які відповідали двом варіантам розташування подвійних зв’язків, було витрачено чимало сил і мистецтва. В жодному разі нічого розділити не вдалося, що і послужило доказом відсутності різких відмінностей між «звичайними» і «подвійними» зв’язками в бензольному кільці.
А потім за пояснення природи хімічних зв’язків взялися фізики, які цей експериментальний факт обґрунтували. І пояснили, чому деякі молекули не можна адекватно відобразити однією традиційною формулою, складеною з ординарних і подвійних рисок. В інших випадках, пояснювали теоретики, можна написати кілька повністю або майже рівноправних формул, які свідчать про властивості складної молекули, лише якщо всі ці формули розглядати в сукупності, разом.
— Ну, це ви киньте! — ось яка була реакція багатьох хіміків-експериментаторів на заяву фізиків.— Якщо формули різні, так і речовини різні.
І знову почалися героїчні, але безплідні спроби розділити те, що не розділяється,— неіснуючі ізомери речовини, що складаються з однакових молекул.
А причина? Те саме переконання, ніби справжня хімія складається тільки в підборі магічних умов, при яких будь-яка речовина, формулу якої придумав хімік, буде стійкою. А всілякі теорії — від лукавого. Небезпека, про яку тільки що говорилося: навіть самий блискучий експериментатор, якщо йому немає справи до теорій та іншої «філософії», ризикує перетворитися у винахідника-маніяка. Чим би він не займався, механікою, хімією чи селекцією рослин.
А ось ще одна небезпека: експериментатор робить справжнє, велике відкриття, знаходить йому задовільне — у рамках своєї «ділянки» — пояснення, а потім заявляє, що виявив закон природи, який скасовує всі раніше діючі закони. Так сталося в кінці позаминулого століття з найбільшим фізикохіміком Вільгельмом Оствальдом.
Вивчаючи поведінку кислот, лугів і солей у водних розчинах, С. Арреніус, В. Оствальд та їх сподвижники довели, що ці речовини здатні розпадатися на заряджені частинки — іони. Були виведені математичні закономірності. Вони чітко зв’язували поведінку іонів з енергією, що виділяється при взаємодії речовини і розчинника. З цих та інших абсолютно вірних фактів і приватних узагальнень Оствальд зробив висновок про те, що… ніяких атомів і молекул взагалі не існує, а існує тільки енергія. Закрив, так би мовити, атомно-молекулярне вчення.
Ще одна історія, пов’язана з фізичною хімією. Навесні 1914 року молодий, незабаром вбитий на війні англійський фізик Р. Мозлі буквально за кілька хвилин довів, що рідкоземельний елемент кельтій в природі не існує. На «відкриття» кельтія французький хімік Ж. Урбен витратив кілька років наполегливої праці, Мозлі ж, ледь глянувши на рентгенівський спектр зразка, цей елемент «скасував»: у спектрі не було жодної нової лінії, кельтій являв собою суміш раніше відомих металів.
Це був один із тріумфів спектроскопії. З тих пір спектроскопічних методів в хімії стало багато, і перемог з їх допомогою здобули незліченну безліч, але були і свої втрати. У деяких хіміків, спокушених швидкодією і порівняно малою трудомісткістю цих методів, з’явилася тенденція «замінювати речовину піками» — всупереч віковим традиціям хімії не виділяти її в індивідуальному вигляді, а обмежитись записом спектроскопічних характеристик. Звичайно, таким шляхом можна швидко довести, що речовина з такою-то формулою в зразку дійсно є, але, по-перше, тут недовго і впасти в помилку, а по-друге, реальні властивості речовини — її стійкість, індивідуальні особливості поведінки — при такій роботі залишаються за бортом. І не раз траплялося так, що важливі теоретичні висновки робили на основі помилкового тлумачення спектру, що з’єднання, про синтез якого переможно повідомляли, виявлялося лише одним з компонентів нероздільної суміші. Ось ще одна грань все того ж одвічного гріха: перебільшення, обожнювання можливостей того чи іншого чудодійного методу.
Ну куди тут дінешся від широкої теорії?
Притча про викрутку
Хімічний синтез, хитромудрі методи спектроскопії, теоретичні побудови, все це інструменти дослідження. Звичайно, поганий працівник, який не знає про існування того чи іншого інструменту, але хіба цим справа обмежується? Хіба назвеш майстром того, хто забиває цвяхи стамескою або свердлить отвори викруткою? Зрозуміло, що кожен інструмент придатний тільки для певного виду робіт. Перша ознака, за якою можна відрізнити вченого від дилетанта, вже була названа — знання напам’ять табу, накопичених наукою за століття свого розвитку. Проте ця ознака, як кажуть математики, необхідна, але недостатня. Більшість табу можна порівняти із заборонними знаками вуличного руху — десь вони з’являються, а далі, через скільки метрів або кілометрів, з’являється знак скасування заборони. Так от, вченому треба знати не тільки про існування табу, але й про межі їх дії.
Таке знання не завжди дається в готовому вигляді — пошуки меж завжди були найбільш привабливою частиною вишукувань експериментаторів, і часом чуття передує знанню. Звідки знав П. Ерліх, що серед сполук миш’яку обов’язково знайдеться «магічна куля», що вбиває шкідливу бацилу? Звідки знав А. Байєр, що барвник індиго обов’язково вдасться синтезувати штучно? Та не могли вони цього знати, але відчували, вірили в свої сили і в могутність хімії.
Автор: П. Савко.

